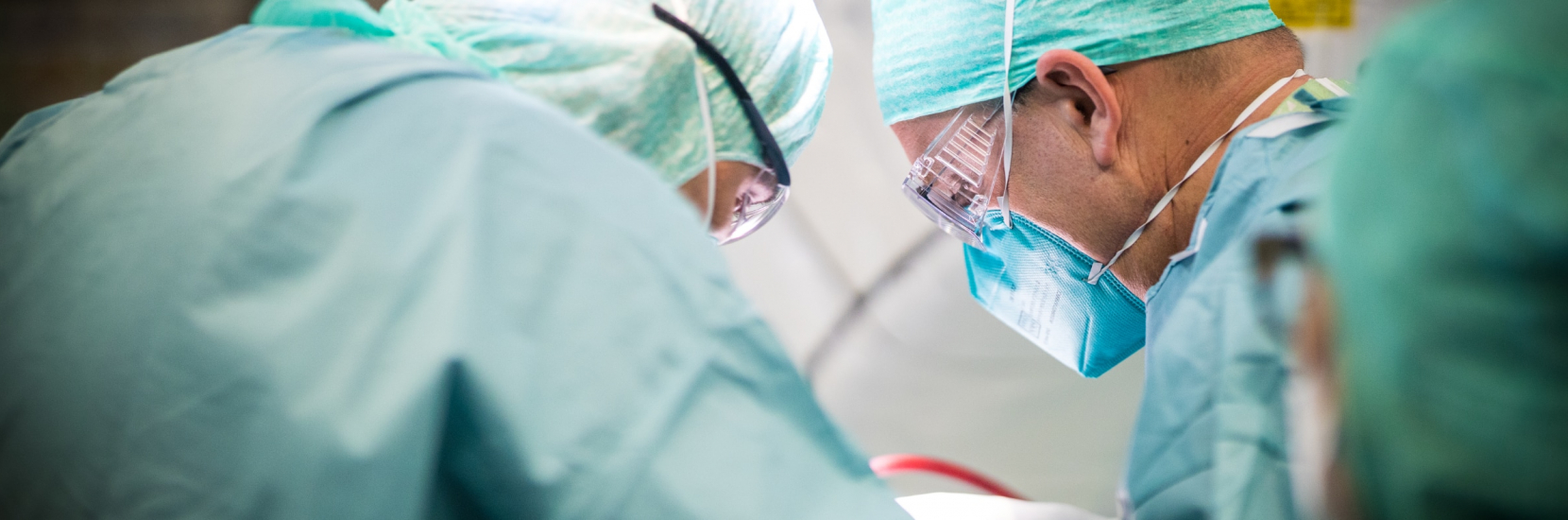
Le service de neurochirurgie du CHL est le service de référence national pour la neurochirurgie. À ce titre, il accueille les patients qui présentent des maladies affectant le cerveau, la colonne vertébrale ou le système nerveux périphérique susceptibles d’être traitées par un acte chirurgical. Au cours d’un entretien passionnant pour MedinLux (journal mensuel distribué aux médecins et pharmaciens), le Pr Frank Hertel, chef du service national de chirurgie au CHL, et Patrick Feltgen, cadre soignant chef d’unité, ont abordé quelques-unes des techniques de pointe qui sont utilisées et/ou développées dans le service afin de réaliser des interventions plus sûres et plus efficaces.
Quelques généralités à propos du service
Le service de neurochirurgie est un service national, qui est de garde pour les urgences neurochirurgicales 24h/24h. Il travaille en étroite collaboration avec les services de neuroradiologie diagnostique et interventionnelle, de neurologie et de réanimation - soins intensifs médico-chirurgicaux.
L’équipe pluridisciplinaire prend en charge les maladies aiguës et chroniques, en collaboration avec les réseaux d’aide et de soins extérieurs.
Les affections traitées par le service national de chirurgie du CHL sont nombreuses : hernie discale, canal lombaire étroit, canal carpien, névralgie du trijumeau, traumatisme crânien, tumeur du cerveau et de la moelle épinière…. On peut dès lors mieux se rendre compte de l’étendue et de la variété des interventions qui sont proposées dans ce service. La quasi-totalité des méthodes et techniques utilisées en neurochirurgie y sont en effet pratiquées. Cela comprend donc les techniques chirurgicales crâniennes minimalement invasives, la chirurgie de la colonne par neuronavigation, la chirurgie endoscopique, les techniques endovasculaires (artériographies/ embolisations), neuroradiologiques, ainsi que la radiothérapie stéréotaxique (CyberKnife; Centre François Baclesse). Tant les adultes que les enfants sont pris en charge.
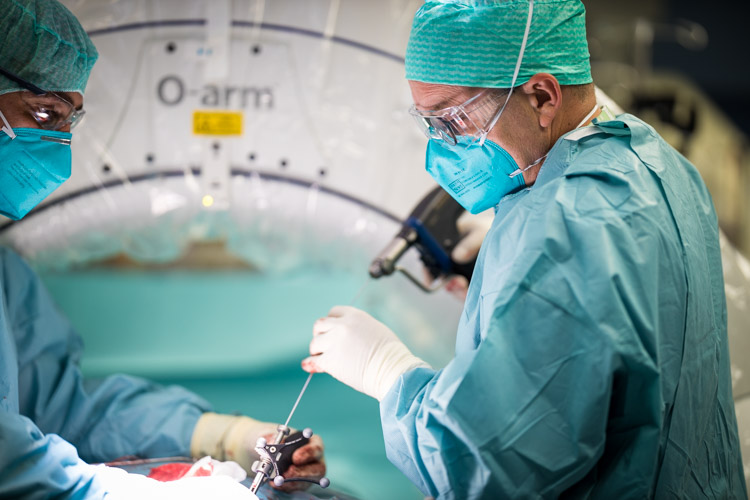
Cet article est l’occasion de vous présenter quelques-unes des techniques qui illustrent à la fois la grande complexité des interventions de neurochirurgie, le recours à des technologies de pointe, les nécessaires collaborations avec d’autres services/spécialités, et, surtout, l’évolution vers des interventions minimalement invasives, qui visent à préserver les tissus cérébraux et leurs fonctions.
- Le neuromonitoring intra-opératoire. Ce monitoring permet de surveiller le système nerveux central lors des opérations neurochirurgicales, avec l’objectif de réduire le risque de déficits post-opératoires.
- La chirurgie d’exérèse guidée par fluorescence. Les glioblastomes sont les tumeurs primitives du système nerveux central les plus fréquentes et les plus agressives. Leur prise en charge repose avant tout sur l’exérèse chirurgicale optimale lorsqu’elle est envisageable, suivie d’une radio-chimiothérapie. La chirurgie d’exérèse guidée par fluorescence a montré, dans plusieurs études, son efficacité pour améliorer la qualité de l’exérèse. Elle permet ainsi d’augmenter de manière significative la survie globale, la qualité de vie et l’efficacité du traitement complémentaire.
- La prise en charge endovasculaire des anévrismes. Lorsqu’un anévrisme cérébral est détecté de manière fortuite et selon le risque estimé de rupture, il peut être surveillé ou traité préventivement. Le risque de rupture est très faible (environ 1/10.000 habitants/an), mais il s’agit d’un événement grave, mortel dans près de la moitié des cas, qui nécessite alors une prise en charge urgente. Plusieurs techniques peuvent être utilisées pour «neutraliser» l’anévrisme, la plus fréquente étant le clippage du col de l’anévrisme, qui implique toutefois une craniotomie. L’alternative est une approche endovasculaire, où l’anévrisme est atteint et traité grâce à un cathéter. Différents matériels peuvent être déployés via ce cathéter, seuls ou en combinaison, pour occlure l’anévrisme ou reconstruire l’artère:
- les coils (implant en forme de fil métallique très souple) ou les plugs (micro- cages grillagées en métal) servent à boucher l’anévrisme;
- les stents à mailles larges, utilisés en complément, permettent de renforcer l’artère;
- les stents à mailles serrées (appelés stents à diversion de flux) qui entraînent progressivement une occlusion (par thrombose) de l’anévrisme.
Ces techniques mini-invasives semblent supérieures en termes de morbi-mortalité et sont à considérer en première intention. L’hétérogénéité de la présentation des anévrismes (état, forme, localisation, taille, taille du collet...) justifie le fait que diverses approches doivent être envisagées pour traiter les différents «types» d’anévrismes intracrâniens par voie endovasculaire, ou qu’il faut discuter leur prise en charge chirurgicale. Ces prises en charge impliquent à la fois des opérateurs du service (chirurgiens et chirurgiens endovasculaires) et des neuro-radiologues.
- La stimulation cérébrale profonde pour traiter l’anorexie mentale. La stimulation cérébrale profonde est l’une des méthodes de traitement de plus en plus utilisées ces dernières années pour traiter l’anorexie mentale, lorsque le pronostic vital de la personne est engagé. Elle permet une meilleure prise de poids et une augmentation subjective de la qualité de vie des patient(e)s.
- Diminuer la (longue) souffrance des patients atteints de névralgie du trijumeau. La douleur est le signe cardinal de la maladie. Elle est décrite comme une décharge électrique qui se manifeste par de brèves salves non prévisibles. La névralgie essentielle du trijumeau requiert un traitement par anticonvulsivants. En cas d’échappement (et/ou d’intolérance) à ces médications, les méthodes chirurgicales actuelles permettent d’apporter la guérison dans la plupart des cas. Mise au point dans les années 60, la décompression vasculaire microchirurgicale au niveau de l’angle ponto-cérébelleux en est la première option, car elle s’adresse à la cause et est conservatrice.
- Des interventions otoneurochirurgicales. Le neurome de l’acoustique est une tumeur bénigne (non cancéreuse) qui se développe le plus souvent aux dépens du contingent vestibulaire du nerf acoustique. Il est responsable d’une surdité souvent difficile à appareiller, de troubles de l’équilibre et d’une possible compression d’autres nerfs crâniens. Dans la majorité des cas, l’évolution de la tumeur est extrêmement lente. Certains neuromes sont donc simplement surveillés de façon régulière, sans aucune intervention chirurgicale. Dans d’autres cas, une ablation chirurgicale de la tumeur est requise. Il s’agit d’une chirurgie particulière, qui peut être particulièrement longue (10-16h en fonction des tissus infiltrés par la tumeur) et s’appuyer sur une double équipe chirurgicale (associant un ORL et un neurochirurgien). Les risques opératoires comprennent une perte complète et définitive de l’audition du côté opéré (fréquente) et la survenue en post-opératoire d’une paralysie faciale, raison pour laquelle ces interventions sont réalisées en utilisant un neuromonitoring du nerf facial. Une radiothérapie peut quant à elle être envisagée pour les tumeurs de petits ou moyens volumes.
- Améliorer la qualité de la stimulation cérébrale profonde (SCP). La stimulation cérébrale profonde est une intervention basée sur l’implantation d’électrodes permanentes dans le cerveau humain pour soulager les symptômes de divers troubles du mouvement et neuropsychiatriques, tels que les tremblements, la dystonie et la maladie de Parkinson. La qualité de la stimulation profonde pourrait cependant être améliorée. Raison pour laquelle, le Pr Hertel collabore avec plusieurs équipes d’informaticiens, notamment pour la conception d’outils plus performants servant à mieux identifier les zones du cerveau qu’il faut cibler.
- Des capteurs de pression dans les chaussures. Un système de capteurs de pression a été conçu pour se placer dans des chaussures que les patients sont invités à porter durant 4 jours. Ce système enregistre tous les mouvements. Leur analyse permet de réaliser des diagnostics différentiels (entre Parkinson et d’autres troubles de la marche), d’évaluer l’efficacité de certains traitements (SCP...), mais aussi de suivre certaines maladies et de documenter certaines indications, comme une éventuelle chirurgie de correction de la colonne sur la base du calcul du risque de chute.
- Analyser les tissus en peropératoire. La résection d’une tumeur cérébrale nécessite une évaluation minutieuse de la nature et de la malignité du tissu tumoral pendant l’intervention, car c’est sur cette base que l’on décide du degré de radicalité de la chirurgie. Généralement, aucun tissu n’est disponible pour analyse avant l’intervention. L’examen histopathologique peropératoire d’échantillons de tumeurs prend du temps et soumet le patient à une tension importante en raison de l’anesthésie continue et de la chirurgie prolongée, d’où la nécessité de développer des méthodes plus rapides pour un diagnostic approfondi. C’est pourquoi le Pr Hertel et son équipe utilisent la spectroscopie Raman. Cette méthode permet une analyse rapide des échantillons sans avoir à les étiqueter ni à les préparer, ce qui en fait un outil utile pour les applications péri- et intra-chirurgicales. D’autre part, elle pourrait fournir des connaissances importantes sur la biochimie des tumeurs et être utilisée pour une sous-classification des tumeurs, avec un impact potentiel sur les approches thérapeutiques personnalisées (basées sur la biochimie de la tumeur).
- Visualiser les faisceaux neuronaux en cours d’intervention. L’imagerie en tenseur de diffusion (DTI) est une technique d’IRM qui permet la cartographie in vivo de la microstructure et de l’organisation des tissus. Elle offre la possibilité de détecter et de quantifier des anomalies de la substance blanche non visibles en imagerie conventionnelle dans des pathologies cérébrales variées. Elle est également utilisée pour réduire le risque d’endommager les faisceaux de matière blanche lors d’une intervention chirurgicale, y compris à proximité des voies visuelles, plus difficiles à représenter [ce qui a nécessité le recours à une technologie dérivée (HARDI) et le développement d’algorithmes spécifiques.
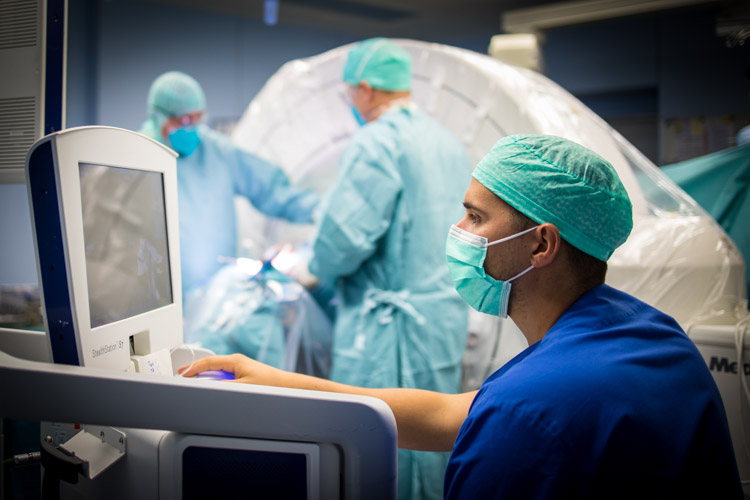
Un travail d’équipe
La pratique de la neurochirurgie implique une organisation complexe, qui doit réunir aux endroits ad hoc les opérateurs, les collaborateurs et le matériel appropriés.
Le team médical comprend 5 spécialistes et 5 assistants. Les séniors peuvent assurer toutes les urgences et les prises en charge standard, mais ont investi chacun une ou plusieurs sous-spécialité(s) (avec un volume suffisant). Sur le plan des soins infirmiers également, les pathologies neurochirurgicales s’avèrent exigeantes.
Pour ne citer qu’un seul exemple, celui du traitement de la douleur par neurostimulation, une dizaine d’appareils différents sont utilisés et doivent donc être connus et maîtrisés par le team infirmier dédié. Comme la neurochirurgie n’est pas enseignée dans le cursus général des soins infirmiers, le team infirmier est formé sur place. Une équipe pluridisciplinaire (kinésithérapeute, ergothérapeute, orthophoniste...) s’occupe de la rééducation précoce. L’objectif est d’intervenir le plus tôt possible afin de profiter de la plasticité cérébrale pour maximiser les chances de récupération après une intervention ou un trauma, par exemple (motricité fine, difficultés de déglutition, aphasie, hémiplégie...), le cas échéant en collaboration avec des structures spécialisées situées en aval, tels le Rehazenter ou le réseau de rééducation gériatrique.
Conclusion
Au cours de la discussion, il est apparu clairement que la quête d’excellence qui prévaut dans le service passe nécessairement par l’acquisition des systèmes les plus récents (techniques numériques de navigation...) – sur ce point, le service est à l’ultrapointe européenne – mais aussi par la formation continue du personnel et d’indispensables collaborations avec d’autres services médicaux du CHL et extra-CHL, ainsi que par des collaborations interdisciplinaires (informaticiens, mathématiciens...) nationales et internationales. Le résultat consiste en des interventions de plus en plus ciblées, tenant compte des particularités de chaque patient (médecine personnalisée) et de sa maladie.
Découvrez l’intégralité de l’article ici.
Source :
MedinLux 2021;18:9-17